Post Relacionados
Analiza proteínas de membrana con XL-MS: Guía de flujo de trabajo paso a paso
2026-02-20Analizar proteínas de membrana con XL-MS es una de las formas más prácticas de convertir interacciones membranarias "difíciles de ver" en evidencia medible. La tecnología Longlight utiliza la reticulación química junto con espectrometría de masas (XL-MS) para ayudar a los investigadores a mapear las interacciones proteína-proteína (IBP), capturar contactos débiles o de corta duración y pasar de hipótesis a modelos estructurales defendibles, sin forzar flujos de trabajo especiales de marcado químico.
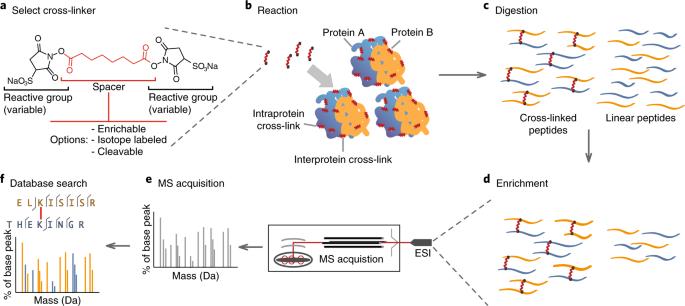
Espectrometría de masas de reticulación: métodos y aplicaciones en estructuras, moleculares y sistemas
¿Qué es XL-MS? ¿Qué son las proteínas de membrana?
XL-MS y las proteínas de membrana son dos ideas que a menudo aparecen juntas en la biología estructural y el descubrimiento de fármacos. Aquí tienes una explicación clara y amigable para principiantes.
¿Qué es XL-MS?
XL-MS significa espectrometría de masas de reticulación (a menudo escrita como reticulación química acoplada a espectrometría de masas).
Es un método utilizado para estudiar las interacciones y formas proteínicas entre proteínas haciendo dos cosas:
Reticulación (XL): "Congelar" las piezas cercanas en su lugar
Un reticulador químico actúa como un pequeño "puente" molecular. Si dos sitios de aminoácidos están lo suficientemente cerca en el espacio real (a corta distancia), el reticulador puede conectarlos covalentemente.
Esto ayuda a preservar interacciones débiles o de corta duración que podrían desintegrarse durante el manejo normal de la muestra.
Espectrometría de Masas (EM): Identificar las piezas enlazadas
Tras la reticulación, las proteínas se digieren en péptidos. El espectrómetro de masas detecta pares de péptidos reticulados y el software los mapea de nuevo a proteínas.
Esos enlaces proporcionan pistas de distancia (restricciones espaciales), indicándote qué regiones estaban cerca en el complejo original.
Lo que te dice XL-MS (en la práctica):
• Qué proteínas probablemente interactúan (red de interacción)
• Qué regiones se tocan (pistas de interfaz)
• Restricciones estructurales que soportan modelos (a menudo combinados con crio-EM o rayos X)
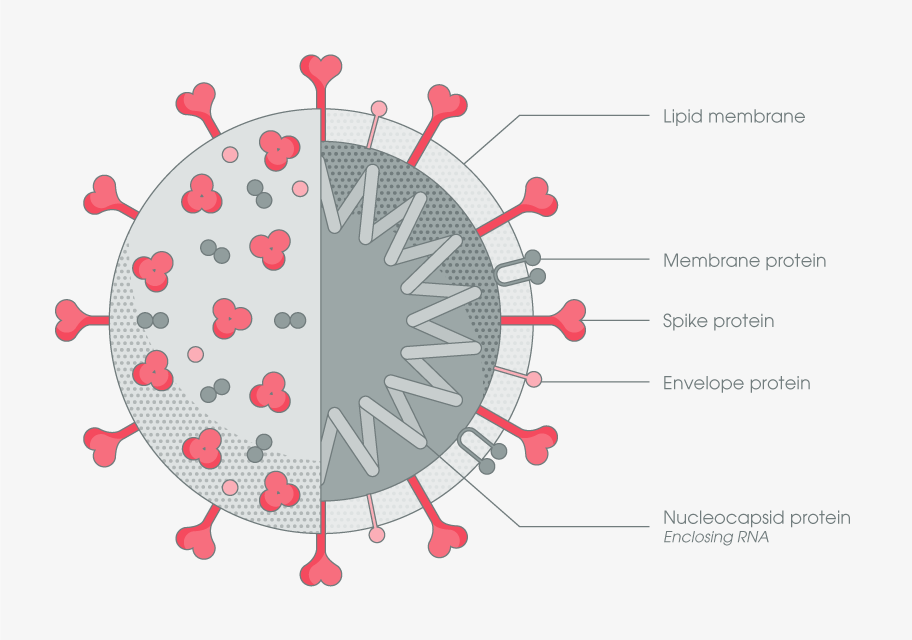
¿Qué son las proteínas de membrana?
Las proteínas de membrana son proteínas que están incrustadas o unidas a una membrana celular (o membranas dentro de células, como el RE, las mitocondrias o las membranas bacterianas).
Son fundamentales porque las membranas controlan el transporte y la señalización, y las proteínas de membrana a menudo actúan como "guardianes" o "antenas" para la célula.
Tipos principales
• Proteínas integrales de membrana: físicamente incrustadas en la membrana
• Muchas abarcan la membrana una o varias veces (a menudo llamadas proteínas transmembrana)
• Proteínas de membrana periférica: adheridas a la superficie de la membrana (a menudo a través de otras proteínas o lípidos)
Por qué importan las proteínas de membrana
• Participan en:
• Transporte (canales, bombas, transportadores)
• Señalización celular (receptores como GPCRs)
• Conversión de energía (complejos de cadena respiratoria)
• Reconocimiento y adhesión celular
Por qué son "difíciles"
Las proteínas de membrana son difíciles de estudiar porque:
• Se asientan en un ambiente lipídico
• Pueden ser inestables cuando se retiran de la membrana
• A menudo forman complejos dinámicos que cambian de estado
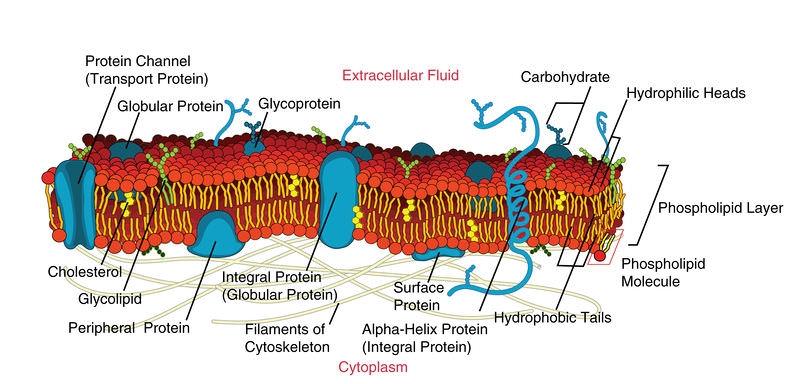
Proteínas de membrana - Biología LibreTexts
Por qué las proteínas de membrana necesitan un Estrategia diferente
Las proteínas de membrana suelen estar en entornos dinámicos y abarrotados. Sus interfaces clave pueden ser transitorias, y muchos complejos son inestables una vez eliminados de la membrana. Por eso los métodos clásicos de interacción pueden pasar por alto contactos críticos o simplificar en exceso lo que está ocurriendo.
Analizar proteínas de membrana con XL-MS funciona porque "congela" las regiones cercanas en su lugar usando agentes de reticulación. Estos reactivos pueden conectar covalentemente dos o más proteínas interactuantes dentro de una ventana de distancia definida. Una vez que la interacción está fijada, la espectrometría de masas puede leer péptidos entrecruzados y señalarte posibles puntos de contacto. Operativamente, la evidencia de interacción sigue siendo rastreable incluso cuando los complejos son débiles.
• Asegura las interacciones de corta duración que a menudo se pierden durante la purificación
• Evita el marcaje químico, simplificando las decisiones tempranas
• Permite la reticulación intracelular para preservar la proximidad nativa
Paso 1: Especificar la cuestión biológica y la justificación de la distancia
Decide qué quieres aprender antes de empezar. ¿Estás confirmando una pareja sospechosa? ¿Comparar la unión mutante frente a la de tipo salvaje? ¿Mapear una interfaz para soportar un modelo? Una pregunta clara te ayuda a elegir condiciones, controles y salidas de datos.
XL-MS es informado por distancia. Los agentes de reticulación conectan residuos que están cerca en el espacio, no necesariamente adyacentes en secuencia. Para las proteínas de membrana, esta lógica de distancias es valiosa porque puede revelar cómo se empaquetan las hélices, cómo los bucles citosólicos contactan a sus compañeros o cómo se ensamblan los oligómeros.
Una forma amigable para principiantes de enmarcar tu plan es definir tres salidas:
• Interacción Presencia: ¿A contacta con B?
• Topología de interacción: ¿qué regiones de A contactan con qué regiones de B?
• Evidencia del lugar: ¿qué pares de péptidos apoyan la red de interacción?
Analizar proteínas de membrana con XL-MS resulta mucho más fluido cuando predecides cuáles de estas necesitas para tu siguiente decisión (modelado estructural, validación de objetivos o estudio de mecanismos).
Paso 2: Elige un Enfoque de reticulación que encaja con el contexto de la membrana
Las proteínas de membrana son sensibles a detergentes, miméticos lipídicos y composición de tampón. El objetivo es mantener un estado que se parezca lo máximo posible al complejo funcional y luego encruzilarse en el momento adecuado.
En Longlight Technology, los clientes pueden enviar muestras ya encruzadas o contactarnos para desarrollar un plan de reticulación y luego enviar muestras. Esta flexibilidad es importante para los objetivos de membrana porque un proyecto puede requerir reticulación en solución, mientras que otro se beneficia de condiciones más nativas o incluso de reticulación intracelular.
✔ Un alto rendimiento y una velocidad de análisis rápida pueden acortar los ciclos de iteración
✔ La reticulación intracelular puede reducir los artefactos derivados de complejos sobregestionados
✔ No existe un requisito especial de etiquetado que mantenga accesibles los primeros experimentos
Consejo práctico para principiantes: planifica al menos un control negativo (sin entrecruzamiento, ni proteína asociada) y una referencia de "comportamiento conocido" si está disponible. Los controles te ayudan a distinguir señales reales de proximidad de las de fondo.
Paso 3: A partir de proteínas entrecruzadas to Péptidos Detectables
Tras la reticulación, el flujo de trabajo debe traducir proteínas en una mezcla de péptidos que conserve la información de la reticulación. Aquí es donde muchos principiantes se sienten perdidos, porque los péptidos reticulados son más raros que los péptidos normales y pueden ser más difíciles de detectar.
Nuestro flujo de trabajo estándar de servicio cubre toda la cadena:
• Digestión enzimática
• Enriquecimiento de péptidos
• Detección por espectrometría de masas
• Análisis de datos
• Entrega de informes experimentales
La idea clave es sencilla: la digestión convierte las proteínas en péptidos, el enriquecimiento aumenta la visibilidad relativa de las especies entrecruzadas, y la espectrometría de masas mide las masas y fragmentos peptídicos para que el software pueda asignar pares de enlace.
Analizar proteínas de membrana con XL-MS es más eficiente cuando se trata la preparación de muestras como un paso de preservación de información, no solo como un protocolo rutinario. Los mejores resultados provienen de una digestión estable y un enriquecimiento cuidadoso para que los datos transmitan suficiente señal para una interpretación segura.
Paso 4: Lectura de espectrometría de masas unnd Interaction Network Mapping
La espectrometría de masas hace más que "identificar proteínas". En XL-MS, identifica pares de péptidos reticulados, que puedes interpretar como restricciones espaciales. Una vez que tienes suficientes enlaces de alta confianza, puedes empezar a representar redes de interacción e inferir sitios de acción, especialmente útil para ensamblajes de membranas complejos.
Aquí es también donde XL-MS se convierte en un puente hacia la biología estructural. Muchos equipos utilizan salidas XL-MS junto con crio-EM o cristalografía de rayos X. La evidencia de la vinculación cruzada puede ayudar:
• Validar si un modelo estructural es plausible
• Resolver orientaciones ambiguas de subunidades
• Soporte para la colocación de dominios cuando la densidad es limitada
En otras palabras, Analizar Proteínas de Membrana con XL-MS puede llevarte de "creemos que estas dos regiones interactúan" a "tenemos evidencia respaldada por distancias que limita el modelo."
Paso 5: Cómo to Lee tInforme uny convertir los datos en próximos experimentos
Un informe solo es valioso si guía las decisiones. Para principiantes, la forma más útil de leer los resultados de XL-MS es buscar patrones, no solo listas.
Empieza con tres preguntas:
✔ ¿Son reproducibles los enlaces cruzados entre réplicas o condiciones? La reproducibilidad genera confianza.
✔ ¿Los enlaces se agrupan en regiones específicas? El agrupamiento a menudo apunta a interfaces reales.
✔ ¿Las condiciones mutantes/ligandos cambian el patrón de enlace? Los cambios pueden revelar mecanismos.
Luego traslada la evidencia a los siguientes pasos. Si los enlaces soportan una interfaz específica, puedes diseñar mutaciones puntuales para validación. Si los enlaces sugieren parejas inesperadas, puedes planificar una confirmación ortogonal. Si los enlaces limitan un modelo, puedes proceder a un refinamiento estructural con mayor confianza.
CTA: Si quieres analizar proteínas de membrana con XL-MS pero no tienes claro cómo elegir condiciones o controles, contacta con Longlight Technology para desarrollar un plan de entrecruzamiento y recibir un informe completo de flujo de trabajo, desde la digestión hasta el análisis de datos. Solicita un presupuesto gratuito para comenzar tu proyecto con una hoja de ruta experimental clara y amigable para principiantes.
¿Por qué Longlight Technology? fo XL-MS uny Más allá
Los proyectos de proteínas de membrana rara vez funcionan en una sola técnica. Normalmente requieren una mentalidad de plataforma: manejo fiable de las muestras, datos rigurosos y herramientas que aceleren la iteración.
Longlight Technology ofrece soporte integral con soluciones genómicas de vanguardia, instrumentos de laboratorio avanzados y reactivos y consumibles de alta calidad diseñados para mejorar la eficiencia y precisión en los laboratorios modernos. Además de los servicios XL-MS, apoyamos a los equipos de investigación con herramientas de genómica y biología molecular, incluyendo instrumentos relacionados con NGS como sistemas de ultrasonicación enfocada, además de consumibles y kits ampliamente utilizados (geles de agarosa prefabricados, kits de extracción de ácidos nucleicos y kits de preparación de bibliotecas) para aplicaciones académicas, clínicas e industriales.
Analizar proteínas de membrana con XL-MS no es solo un método, es una disciplina de flujo de trabajo. Cuando el flujo de trabajo es estable, tus conclusiones se vuelven más claras, tus modelos más defendibles y tu próximo experimento se vuelve más fácil de diseñar.