Post Relacionados
Resolución de problemas de ChIP-Seq 101: Arreglar la baja señal paso a paso
2026-02-28La solución de problemas en ChIP-Seq suele comenzar con un síntoma sencillo: baja señal, pero las causas reales suelen distribuirse en la calidad de la cromatina, el rendimiento de los anticuerpos, las condiciones de inmunoprecipitación y la calidad de calidad de la biblioteca. En Longlight Technology, apoyamos laboratorios que ejecutan ChIP-Seq para marcas de histonas y factores de transcripción, y vemos que los mismos "puntos de fallo silenciosos" se repiten en diferentes instrumentos y tipos de muestras. Esta guía básica de solución de problemas de ChIP-Seq guía a los principiantes paso a paso para recuperar la señal en un orden lógico, utilizando puntos de control prácticos que puedes verificar en una sola ejecución.
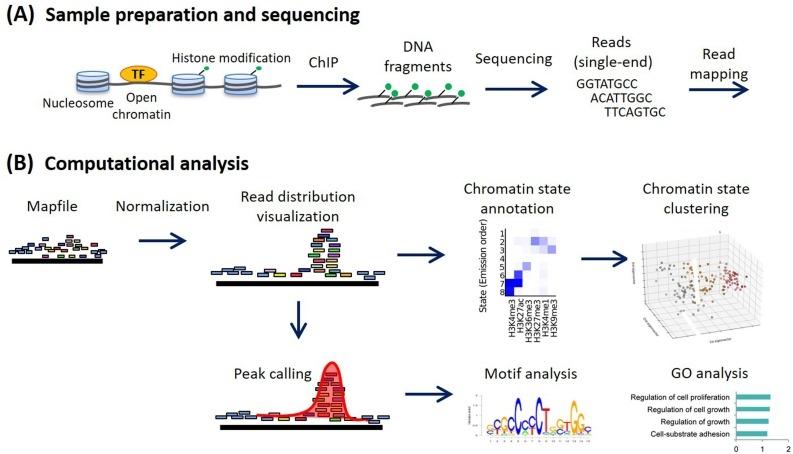
Métodos para el análisis ChIP-seq: Un flujo de trabajo práctico y aplicaciones avanzadas - ScienceDirect
1) Definir "Señal baja" Antes de que cambies nada
Una señal baja puede significar cosas diferentes: muy pocos picos, un enriquecimiento débil en loci conocidos o una biblioteca que parece bien pero que se mapea mal. Buena solución de problemas con ChIP-Seq comienza etiquetando claramente el modo de fallo, porque cada modo apunta a soluciones diferentes.
Una forma amigable para principiantes de definir el problema es comprobar tres capas:
✓ Capa de biología: ¿Está el objetivo presente en tu estado celular (estimulado vs en reposo, fase de diferenciación, momento del tratamiento)?
✓ Capa de enriquecimiento: ¿El ADN ChIP muestra enriquecimiento por qPCR en un locus de control positivo frente a una región negativa?
✓ Capa de secuenciación: ¿Tienes suficientes lecturas únicas y mapeadas y un nivel de duplicado razonable?
Si no puedes responder a estas tres, no "optimices todo". Haz un experimento controlado primero: mantén la muestra igual, mantén la profundidad de secuenciación modesta y cambia solo una variable sospechosa.
2) Empezar con la cromatina: tamaño del fragmento unnd Control de pérdidas
Cuando los laboratorios preguntan por qué un ChIP "no funciona", la causa raíz más común es la cromatina que está sobrefragmentada, poco fragmentada o simplemente perdida durante la limpieza. En la solución de problemas ChIP-Seq, la cromatina es tu base: si es inconsistente, cada paso posterior se convierte en ruido.
Para flujos de trabajo basados en sonicación, muchos laboratorios buscan fragmentos en el rango de ~150–300 pb para llamadas pico agudas y inmunoprecipitación constante. Si los fragmentos son mayormente más grandes (por ejemplo, >500 pb), los anticuerpos tienen dificultades para bajar eficientemente los complejos objetivo. Si los fragmentos son demasiado pequeños, puedes destruir epítopos o aumentar el fondo liberando ADN no específico.
Puntos prácticos de control que puedes hacer inmediatamente:
• Medir el ADN tras la retransmisión inversa y la limpieza (no solo antes de la IP). Una gran caída aquí indica pérdida en cuentas/columnas o condiciones adversas.
• Comparar perfiles de fragmentación entre muestras. Si una muestra es "perfecta" y la siguiente está esfumada o sobredimensionada, céntrate en la lisis y los ajustes de sonicación, no en los anticuerpos primero.
• Conservar una alicuota de "ADN de entrada" de cada lote. Esta es tu base tanto para qPCR como para la QC de bibliotecas.
En Longlight Technology, recomendamos tratar la preparación de la cromatina como un paso controlado de fabricación: fijar la composición del tampón, mantener la temperatura de la muestra estable durante la sonicación y registrar los ajustes exactos del ciclo. Pequeñas desviaciones crean grandes diferencias en la resistencia máxima más adelante.
3) Ajuste de anticuerpos: especificidad, variación del lote, unnd Controls
Si la cromatina parece razonable, el siguiente paso en la solución de problemas de ChIP-Seq es la selección y validación de anticuerpos. La baja señal suele ser causada por el uso de un anticuerpo que es "bueno para occidente" pero débil para ChIP, o por la variabilidad de un lote a otro.
Una buena estrategia de anticuerpos se basa en los controles:
✓ Objetivo de control positivo: una marca de histonas con enriquecimiento robusto (comúnmente utilizada para confirmar la salud del flujo de trabajo).
✓ Control negativo: IgG o un control isotipo para estimar el pull-down de fondo.
✓ Loci conocidos qPCR: uno o dos loci positivos publicados para tu objetivo, más una región desértica genética.
Para los factores de transcripción, la señal puede ser inherentemente inferior a las marcas de histonas. Eso significa que tu anticuerpo debe ser de alta afinidad y tus condiciones IP deben estar limpias. Si eres nuevo en TF ChIP, no empieces cambiando la profundidad de secuenciación. Primero confirma el enriquecimiento mediante qPCR. Si el enriquecimiento qPCR es débil, más lecturas te darán más ruido.
Consejo práctico: Cuando cambies de lote de anticuerpos, revisa el enriquecimiento en el mismo lote de cromatina si es posible. Si el cambio de parcela se rompe la señal, el flujo de trabajo no es necesariamente "incorrecto": el rendimiento de tu reactivo ha cambiado, y tu camino de solución de problemas debería reflejar eso.
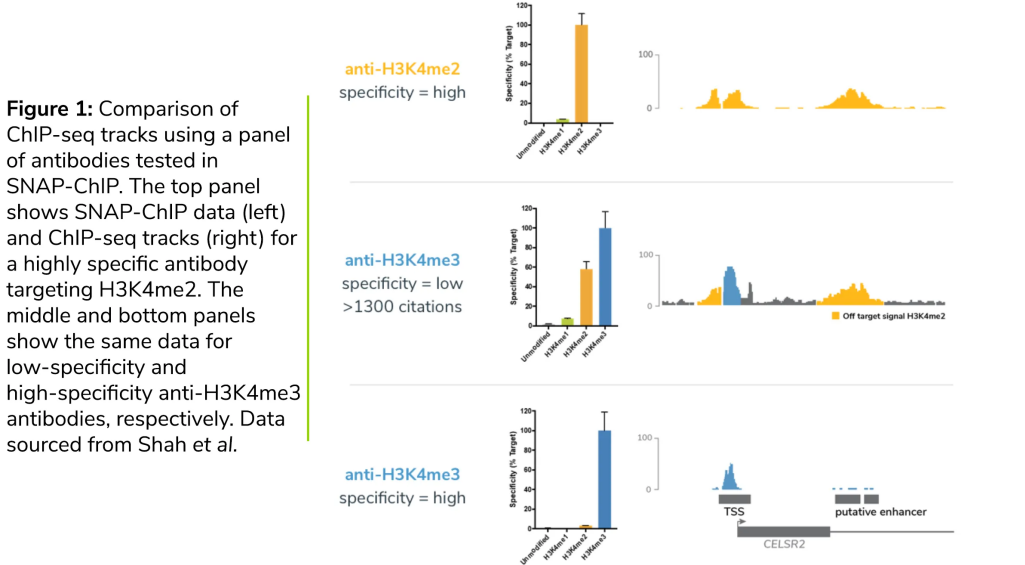
Elegir el anticuerpo ChIP adecuado para tu experimento - EpiCypher
4) Secuencia limpia de optimización de IP—sin conjeturas
Más allá de la cromatina y los anticuerpos, la química IP (perlas, lavados, incubación) es el siguiente punto caliente. La baja señal suele ser un problema de fondo.
✓ Selección de cuentas: Elige la proteína A/G que se adapte a tu especie o isotipo de anticuerpos.
✓ Cantidad de anticuerpos: Titular para evitar un débil pull-down o un aumento elevado de ADN inespecífico.
✓ Balance de lavado: Calibrar la stringencia para eliminar ruido pero preservar interacciones débiles pero reales.
Una regla práctica para principiantes es ajustar solo un eje por partida:
• Si existen picos pero son débiles, aumenta la captura efectiva (un poco más de anticuerpos, mejor unión de perlas, incubación más larga).
• Si los picos son anchos y ruidosos, aumenta la especificidad (lavados más fuertes, mejor bloqueo, reducción de la sobrecarga de anticuerpos).
Desde la perspectiva del fabricante, Longlight Technology diseña reactivos de inmunoprecipitación y sistemas de perlas magnéticas para minimizar la pérdida durante el manejo, porque la pérdida de muestras se parece exactamente a "baja señal". La separación suave de las perlas, la fijación consistente y los pasos de lavado limpios reducen la variabilidad entre operadores, especialmente importante para los equipos que forman al nuevo personal.
5) Control de calidad de la biblioteca: cuando "Buen ADN" Sigue dando señal baja
A veces el enriquecimiento de ADN ChIP es real, pero los datos finales siguen pareciendo planos. En la resolución de problemas ChIP-Seq, esto suele apuntar a métricas de construcción de bibliotecas o secuenciación.
Causas comunes a nivel de biblioteca de baja señal:
✓ Sobreamplificación: demasiados ciclos de PCR pueden inflar duplicados y reducir lecturas únicas utilizables.
✓ Artefactos adaptadores/cebadores: estos consumen lecturas de secuenciación sin mejorar la cobertura del objetivo.
✓ Pobre complejidad: a menudo causada por muy baja entrada de ADN ChIP o pérdida durante la limpieza.
Qué debes comprobar antes de volver a ejecutar todo el ChIP:
• Distribución del tamaño de la biblioteca (quieres un pico limpio, no múltiples picos inesperados).
• Tasa de duplicación y tasa de mapeo única tras la alineación.
• Tendencia de la fracción de lecturas en picos (FRiP) en relación con tu línea base interna (incluso los principiantes pueden seguir el "mejor vs peor" a lo largo de las bajas).
Si sospechas que hay un sobreciclo de la biblioteca, una mejora sencilla es reducir el recuento de ciclos y aumentar la eficiencia de captura aguas arriba (mejor recuperación de cromatina y especificidad de IP). Secuenciar más a fondo no puede compensar una biblioteca de baja complejidad.
6) Escalón-Por-Recuperación de la señal de pasos puedes empezar mañana
Una secuencia práctica que supera a los ajustes ad hoc:
✓ Paso 1: Verificar que los fragmentos de cromatina estén a ~150–300 bp y confirmar la recuperación de ADN tras el cruce inverso.
✓ Paso 2: Comprueba el enriquecimiento por qPCR en un locus positivo y uno negativo antes de preparar la biblioteca.
✓ Paso 3: Añadir controles adecuados (entrada IgG) para separar "sin enriquecimiento" de "alto fondo".
✓ Paso 4: Ajustar las condiciones IP una variable a la vez (perlas, cantidad de anticuerpos, stringencia de lavado).
✓ Paso 5: Auditar métricas de biblioteca (duplicación, mapeo, distribución de tamaño) antes de asumir que la profundidad de secuenciación es el problema.
CTA (Tecnología de Luz): Si quieres un camino más rápido, contacta con Longlight Technology para una lista de comprobación de solución de problemas ChIP-Seq y una hoja de cálculo de diagnóstico muestra por muestra (biblioteca de → de de cromatina → IP). También podemos recomendar una estrategia de diseño de control y emparejamiento de reactivos para reducir la variabilidad del operador y ayudar a los principiantes a alcanzar un enriquecimiento estable antes.
La señal baja es frustrante, pero rara vez es un misterio. Con un flujo disciplinado de solución de problemas ChIP-Seq —empezando por la integridad de la cromatina, luego el ajuste de anticuerpos, luego la especificidad IP y finalmente la QC de la biblioteca— puedes convertir una ejecución débil en un protocolo repetible que escale entre muestras, personal y proyectos.