Post Relacionados
Qué enseña la EM de entrecruzamiento para complejos proteicos sobre el cambio conformacional
2026-02-22La EM de reticulación cruzada para complejos proteicos es una de las formas más prácticas de "congelar" contactos proteicos reales en su lugar y luego leerlos mediante espectrometría de masas, para que puedas aprender cómo un complejo cambia de forma, no solo cómo se ve en una instantánea. En Longlight Technology, vemos a muchos equipos empezar con una pregunta sencilla: ¿Mi complejo proteico es estático o es el cambio entre conformaciones que importan para la función? Este artículo explica, de forma amigable para principiantes, qué puede enseñarte la reticulación química junto con la espectrometría de masas (a menudo llamada CL-MS o XL-MS) sobre el cambio conformacional, y cómo convertir los resultados en decisiones sobre las que puedes actuar.
Avances en el análisis de complejos proteicos mediante reticulación química junto con espectrometría de masas
1) ¿Qué es la EM?
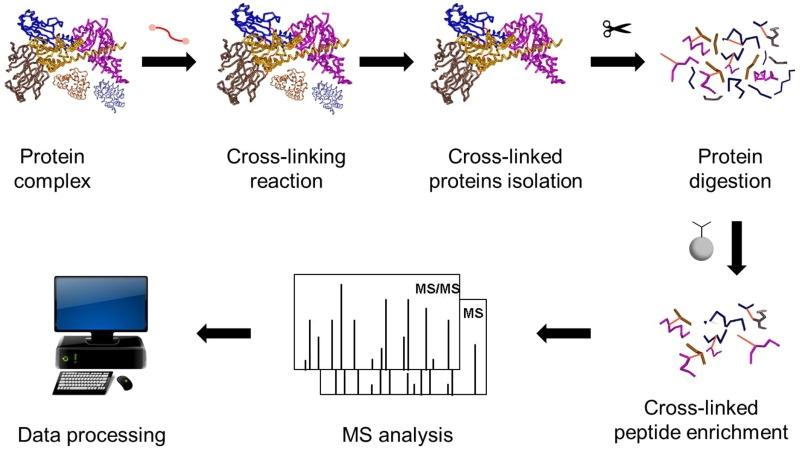
MS de reticulación cruzada (a menudo escrito XL-MS o CL-MS) es un método que ayuda a identificar qué partes de las proteínas están próximas entre sí—ya sea dentro de una proteína o entre proteínas de un complejo—mediante "enlazones" químicamente y luego identificando esos enlaces mediante espectrometría de masas.
Esta es la idea en palabras sencillas:
• Añadir un reticulador (un pequeño "puente" químico)
Reacciona con aminoácidos específicos y puede conectar covalentemente dos residuos que están a una distancia limitada entre sí.
• Digirir las proteínas en péptidos
Las enzimas (a menudo tripsina) cortan las proteínas en pedazos más pequeños.
• Ejecutar espectrometría de masas
La EM detecta péptidos, incluidos pares de péptidos reticulados.
• Analizar los enlaces cruzados
Cada enlace identificado se convierte en una restricción de distancia:
"El Residuo A y el Residuo B estaban lo suficientemente cerca como para estar conectados en estas condiciones."
Para qué se usa
• Mapeo de interacción proteína-proteína (PPI): quién toca a quién en un complejo
• Identificación de la interfaz: qué regiones forman la superficie de contacto
• Cambio conformacional: compara las condiciones (apo vs ligado al ligando, mutante vs WT) para ver que aparecen o desaparecen los contactos
• Soporte para modelado estructural: combinar con crio-EM/rayos X para validar o refinar modelos
Por qué es valioso
• Puede capturar interacciones débiles o de corta duración (el enlace covalente las "congela")
• A menudo no se requiere etiquetado especial
• Puede ser de rendimiento relativamente alto para comparar múltiples condiciones
2) Por qué el cambio conformacional es tan difícil To Captura
Muchos complejos proteicos no permanecen quietos. Respiran, pivotan, abren, cierran y reorganizan las subunidades en respuesta a ligandos, sal, pH, fosforilación o compañeros de unión. Los métodos estructurales tradicionales pueden ser excelentes, pero a menudo favorecen estados estables. Si un complejo es flexible, está mal ensamblado o dura poco, puede que solo veas parte de la historia.
La reticulación ayuda porque puede conectar covalentemente dos residuos que se acercan a cierta distancia. En términos sencillos, indica que "estas dos posiciones estaban lo suficientemente cerca para tocarse" en el momento de la reacción. Las comparaciones de enlaces cruzados lado a lado —sin ligandos frente a ligando, con bajo frente a alto en sal, tipo salvaje frente a mutante— indican si el complejo se compacta, expande o se reconfigura.
✅ Información práctica para principiantes: los desplazamientos conformacionales son cambios de conjunto. XL-MS ve más allá de la conformación más estable hacia el espectro de estados en solución.
Servicio de Espectrometría de Masas de Reticulación | MtoZ Biolabs
Qué mide la EM en la práctica
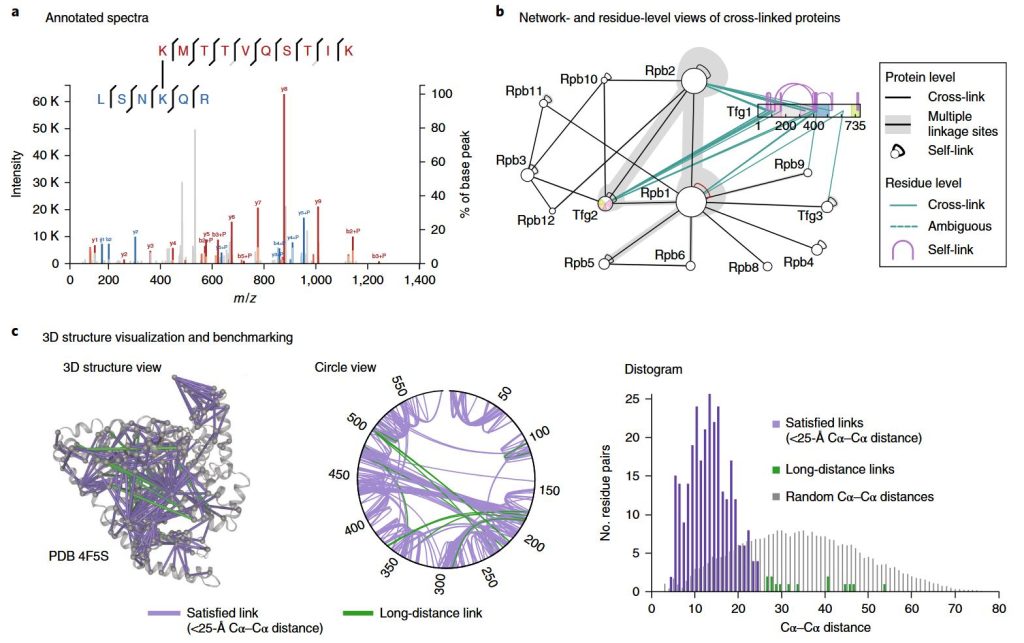
La entrecruzamiento químico con la EM cuantifica la proximidad de residuos y los patrones de interacción, un enfoque estándar para estudiar los IBP. Los agentes de reticulación interactúan con grupos funcionales en proteínas y pueden conectar dos o más proteínas interactuantes (o dos posiciones dentro de una misma proteína). Tras la reticulación, la espectrometría de masas analiza péptidos reticulados, permitiendo representar redes de interacción e identificar los sitios de acción.
¿Qué significa eso para el cambio conformacional?
• Si un conjunto de enlaces cruzados aparece solo después de la unión de ligandos, sugiere que se formaron nuevos contactos en el estado unido.
• Si ciertos enlaces cruzados desaparecen, sugiere que esos sitios ya no están cerca—quizá se abre el complejo o se mueve un dominio.
• Si los enlaces cruzados se desplazan entre subunidad, puede indicar una reorganización de subunidades o una ruta de ensamblaje diferente.
✅ Qué ganas con este método (y por qué importa):
• No se necesita marcaje químico especial → puedes mantener la proteína cerca de su forma original y reducir la sobrecarga experimental.
• Captura interacciones de corta duración y débilidad, → enlaces covalentes pueden preservar contactos que de otro modo se deshacen durante la purificación o análisis.
• Alto rendimiento y velocidad de análisis rápida → útiles cuando se necesitan comparar muchas condiciones o construcciones de forma eficiente.
• La reticulación intracelular es posible → para algunos proyectos, esto ayuda a estudiar complejos más cercanos a su contexto celular nativo que solo in vitro.
4) Lectura "Movimiento" De los patrones de enlace cruzado
Los principiantes a veces esperan que un cruce de enlace equivalga a una respuesta. En la práctica, el valor proviene de los patrones.
Una forma útil de pensar es: los enlaces cruzados son restricciones de distancia. Cuando un complejo cambia de conformación, la distancia entre dos residuos cambia. XL-MS no siempre puede decirte el ángulo exacto de rotación, pero sí puede indicarte si las regiones probablemente se acercaron o se alejaron, y si cambió el mapa de interacción.
Aquí tienes historias conformacionales comunes que XL-MS puede revelar:
✅ Compactación vs Apertura
Si observas más vínculos cruzados intraproteicos que abarcan regiones distantes bajo una condición, la proteína podría estar adoptando un estado más compacto. Si esos enlaces caen mientras otros suben, puede que se esté abriendo.
✅ Conmutación de interfaces
Si los enlaces cruzados entre la subunidad A y B se debilitan, mientras que los enlaces entre A y C se fortalecen, sugiere un conjunto o interruptor de interfaz reponderado.
✅ Estabilización por ligando o mutación
Un ligando que "bloquea" una conformación a menudo aumenta la reproducibilidad de un conjunto específico de reticulo y reduce patrones mixtos.
Desde un punto de vista práctico, esto puede guiar los siguientes pasos: qué mutante crear, qué dominio truncar, qué condición de búfer estabiliza el complejo o qué interfaz validar mediante otro método.
5) Resultados más fuertes cuando XL-MS se combina con crio-EM o rayos X
XL-MS se utiliza a menudo junto con la criomicroscopía electrónica (crio-EM) y la difracción de cristales de rayos X para la investigación de estructuras biológicas. La combinación es especialmente útil cuando el cambio conformacional es la cuestión central.
• La crio-EM puede proporcionar un modelo estructural para los estados dominantes.
• XL-MS puede validar si un modelo es consistente con el comportamiento de la solución y puede señalar estados alternativos que el crio-EM puede submuestrear.
• Rayos X puede ofrecer dominios de alta resolución, mientras que XL-MS ayuda a colocar dominios dentro de un ensamblaje flexible.
✅ Un flujo de trabajo práctico: usa primero XL-MS para saber si tu complejo es heterogéneo. Si es así, puedes diseñar condiciones que enriquezcan un estado antes de invertir mucho en trabajos estructurales de alta resolución.
6) El flujo de trabajo de servicios At Tecnología de Luz Larga
Muchos laboratorios quieren obtener los conocimientos de la EM de reticulación cruzada para complejos proteicos sin tener que construir una cadena completa internamente. Longlight Technology apoya tanto a equipos experimentados como a usuarios primerizos con un proceso de servicio claro.
Puedes enviar muestras reticuladas o contactarnos para desarrollar un plan de reticulación y luego enviar muestras. Completamos todo el flujo de trabajo, incluyendo la digestión enzimática, el enriquecimiento de péptidos, la detección por espectrometría de masas, el análisis de datos y la entrega de un informe experimental. Este enfoque de extremo a extremo es importante porque la interpretación conformacional depende de un manejo consistente a través de los pasos.
✅ Qué significa esto para ti como cliente:
• Menos errores de traspaso entre pasos y menos "incógnitas" al comparar condiciones
• Un informe organizado en torno a interpretaciones accionables, no solo identificaciones en bruto
• Iteración más rápida cuando se necesitan probar múltiples constructos o condiciones de tratamiento
Si tu proyecto más amplio incluye genómica o desarrollo de ensayos a nivel posterior, Longlight también ofrece soluciones genómicas de vanguardia, instrumentos de laboratorio avanzados y reactivos y consumibles de alta calidad diseñados para mejorar la eficiencia y precisión en laboratorios modernos, apoyando flujos de trabajo de investigación desde la biología molecular hasta el análisis de precisión.
7) Un CTA práctico: convertir preguntas conformacionales en pruebas comprobables
El cambio conformacional no es un detalle secundario. A menudo decide si un objetivo es farmacológico, si un complejo se ensambla correctamente y si una mutación es realmente disruptiva. La esclerosis múltiple de enlaces cruzados para complejos proteicos te da pruebas que puedes comparar entre condiciones, lo que te ayuda a dejar de adivinar y empezar a diseñar.
✅ Si planeas un estudio de cambio conformacional, considera empezar con un "conjunto de comparación":
• Apo vs ligado al ligando (o al inhibidor)
• Mutante de tipo salvaje vs mutante de una interfaz
• Un tampón estabilizador frente a un tampón de estrés (rango sal/pH)
CTA: Si quieres un plan XL-MS claro y amigable para principiantes adaptado a tu complejo proteico, contacta con Longlight Technology para hablar de tu objetivo (mapeo de interacción, validación de interfaces o comparación conformacional). Podemos ayudarte a elegir una estrategia práctica de entrecruzamiento y entregar un informe interpretable que apoye tu próximo experimento—o tu próximo modelo estructural.